Uno studio recente pubblicato inmicrobiomaÈ stata condotta un'analisi metagenomica virale su 846 piccoli mammiferi selvatici, tra cui pipistrelli, roditori e toporagni, raccolti in Sierra Leone, Africa occidentale. Lo studio ha identificato un totale di 39 virus a RNA associati ai mammiferi, di cui 26 nuovi e 13 già noti. Tra questi, la famiglia Paramyxoviridae ha mostrato la maggiore diversità, mentre i roditori ospitavano il maggior numero di specie virali (n = 26).
La valutazione del rischio zoonotico ha rivelato la presenza di tre virus zoonotici noti: il virus dell'encefalomiocardite, il virus di Lassa e il Rocahepevirus sp., oltre a tre virus con potenziale rischio di spillover: il virus Melian, il virus dell'epatite dei roditori e l'Hunnivirus A. In particolare, tra i virus di nuova identificazione, il Bat ledantevirus 2 ha mostrato la più stretta relazione filogenetica con il virus Le Dantec, che infetta l'uomo. L'analisi sierologica ha inoltre rilevato anticorpi neutralizzanti contro questo virus nel 2,8% dei residenti locali, suggerendo una precedente esposizione umana, probabilmente non rilevata.
Questi risultati evidenziano la presenza di un consistente serbatoio virale dominato dai roditori nell'Africa occidentale e sottolineano l'importanza cruciale di strategie di sorveglianza integrate all'interfaccia uomo-animale. La combinazione dello screening metagenomico con la validazione sierologica fornisce un quadro solido per l'identificazione di virus con potenziale zoonotico e di spillover.

Nell'ultimo decennio, oltre il 60% delle malattie infettive emergenti nell'uomo ha avuto origine da serbatoi animali, con pipistrelli, roditori e toporagni riconosciuti come ospiti chiave di virus zoonotici. L'Africa è ampiamente considerata un focolaio di malattie zoonotiche. Ad esempio, la Sierra Leone ha segnalato oltre 28.000 casi durante l'epidemia di Ebola del 2014-2016.
Nonostante il significativo carico di malattie zoonotiche in questa regione, la diversità e la distribuzione dei virus nei piccoli mammiferi selvatici rimangono insufficientemente caratterizzate. Per colmare questa lacuna, i ricercatori hanno condotto un'analisi sistematica del viroma di 846 piccoli mammiferi selvatici catturati in tre siti della Sierra Leone tra il 2018 e il 2023. Lo studio si proponeva di caratterizzare la diversità virale, identificare i candidati con potenziale di trasmissione interspecie, valutare il rischio zoonotico e generare dati a supporto dei sistemi di allerta precoce per le malattie infettive emergenti.
Metodi principali
Lo studio ha applicato un flusso di lavoro completo di metagenomica virale:
- Elaborazione del campione:Tessuti di cuore, fegato, milza, polmone e rene sono stati raccolti, riuniti, omogeneizzati e sottoposti all'estrazione dell'RNA totale.
- Sequenziamento e assemblaggio:La deplezione dell'RNA ribosomiale è stata eseguita prima della costruzione della libreria, seguita dal sequenziamento ad alto rendimento utilizzando la piattaforma Illumina NovaSeq 6000. I contig virali sono stati assemblati de novo.
- Identificazione del virus:I virus sono stati identificati in base all'allineamento del gene della RNA polimerasi RNA-dipendente (RdRp). Sono stati mantenuti solo i virus associati ai vertebrati, escludendo i virus batterici, fungini e vegetali.
- Analisi bioinformatica:Sono state condotte ricostruzioni filogenetiche, analisi di ricombinazione, modellizzazione di reti di trasmissione interspecifica e valutazione del rischio zoonotico.
- Validazione sierologica:È stato sviluppato un test di neutralizzazione pseudovirale basato sul virus VSV per il Bat ledantevirus 2. Anticorpi neutralizzanti sono stati rilevati nel 2,8% dei sieri umani, fornendo prove di una potenziale trasmissione zoonotica.
StudioRisultati
1. Scoperta e diversità virale
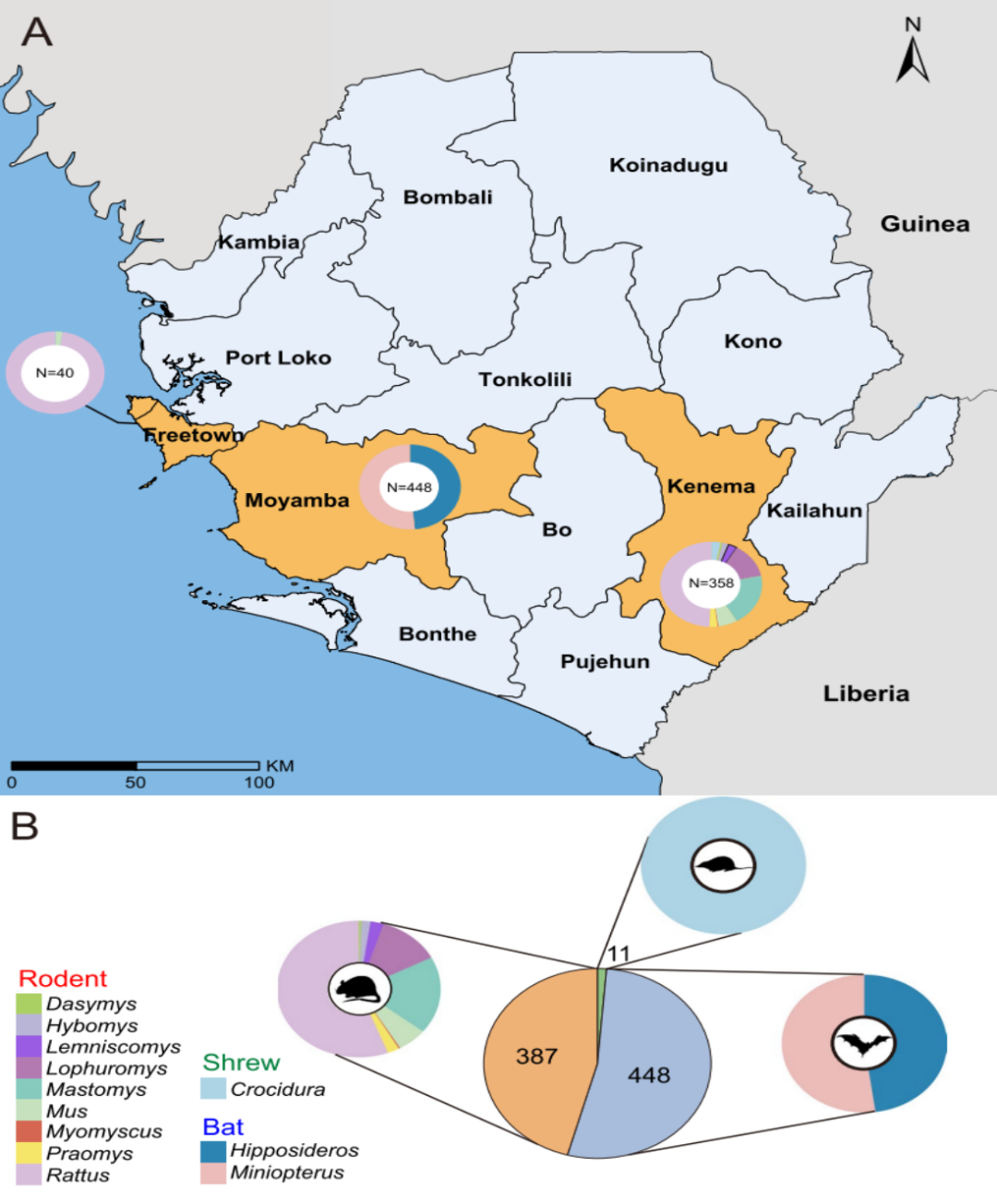
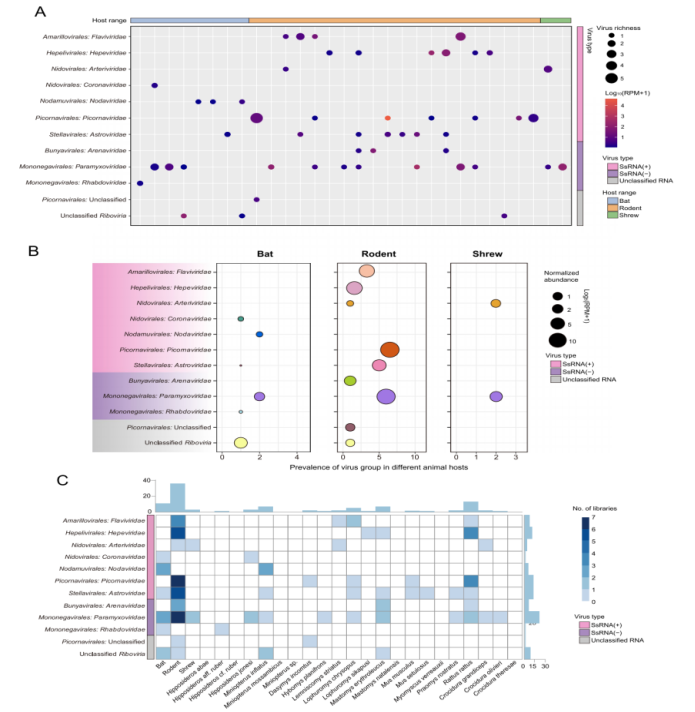
Questo studio ha condotto un'analisi di sequenziamento trascrittomico su 846 animali selvatici raccolti in Sierra Leone, tra cui roditori, pipistrelli e toporagni. Sulla base delle sequenze complete del gene della RNA polimerasi RNA-dipendente (RdRp), sono stati identificati un totale di 39 virus a RNA associati ai mammiferi, di cui 13 già noti e 26 nuovi.
In termini di composizione virale, la famiglia Paramyxoviridae ha mostrato il più alto livello di diversità in tutti e tre gli ordini di ospiti, seguita da Astroviridae e Picornaviridae. Per quanto riguarda la distribuzione degli ospiti, i roditori hanno contribuito alla maggiore diversità virale, ospitando un totale di 26 specie virali, a dimostrazione del loro ruolo preminente come serbatoi di diversità virale nella regione.
2. Rischio zoonotico
La valutazione del rischio zoonotico ha identificato tre virus zoonotici noti: il virus dell'encefalomiocardite, il virus di Lassa e le specie di Rocahepevirus. Inoltre, tre virus – il virus di Melian, il virus dell'epatite dei roditori e l'Hunnivirus A – sono stati identificati come potenzialmente a rischio di spillover.
Tra i 26 virus appena scoperti, quattro sono stati considerati ad alto potenziale zoonotico in base alle caratteristiche filogenetiche e genomiche. In particolare, il Bat ledantevirus 2 ha mostrato la più stretta relazione filogenetica con il virus Le Dantec, noto per infettare l'uomo.
Successive indagini sierologiche hanno ulteriormente confermato questo risultato, rilevando anticorpi neutralizzanti contro il Bat ledantevirus 2 nel 2,8% dei sieri dei residenti locali. Questo dato suggerisce che infezioni non riconosciute o asintomatiche potrebbero essersi già verificate nella popolazione umana, evidenziando una potenziale via di trasmissione zoonotica finora non rilevata.
3. Dinamiche di trasmissione interspecie
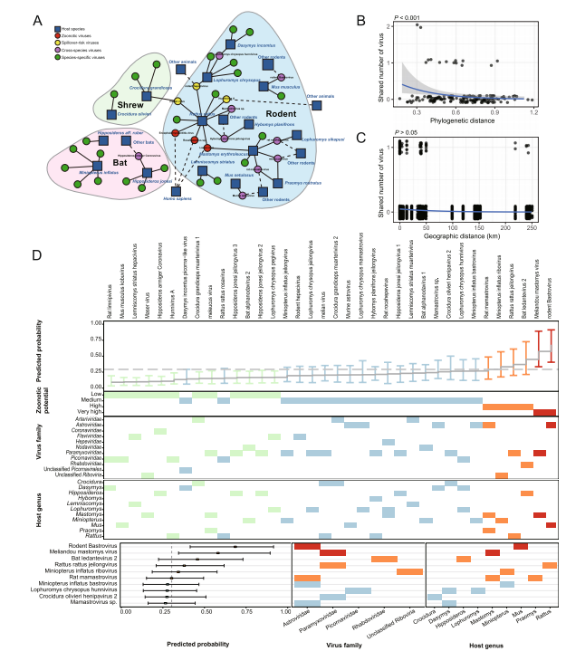
L'analisi della trasmissione interspecie ha dimostrato che i roditori occupano una posizione centrale all'interno della rete di condivisione virale, agendo come nodi chiave che facilitano lo scambio virale tra le specie ospiti. Sono stati identificati in totale 15 virus con potenziale di trasmissione interspecie.
Ulteriori analisi dei modelli di trasmissione tra ordini diversi hanno indicato che la condivisione virale si verificava più frequentemente tra ospiti appartenenti allo stesso ordine tassonomico, suggerendo che la parentela tra gli ospiti gioca un ruolo importante nelle dinamiche di trasmissione. Al contrario, i pipistrelli hanno mostrato una capacità relativamente inferiore di trasmissione tra ordini diversi.
È importante sottolineare che in alcuni virus è stata osservata un'espansione della gamma di ospiti. Ad esempio, il virus Melian, precedentemente considerato specifico dei toporagni, è stato rilevato anche nei roditori in questo studio, indicando un potenziale cambiamento nell'adattabilità dell'ospite e un aumento del rischio di trasmissione più ampia.
Conclusioni e implicazioni per la salute pubblica
- Elevata diversità del viroma nei piccoli mammiferi selvatici:La scoperta di 39 virus a RNA, tra cui 26 nuove specie, rivela un ampio serbatoio virale nella regione e segnala per la prima volta nuovi virus con un elevato potenziale zoonotico (ad esempio, Bat ledantevirus 2).
- I roditori come obiettivi prioritari di sorveglianza:I roditori fungono da snodi fondamentali per la trasmissione virale e presentano la più alta diversità virale, rappresentando quindi il rischio maggiore di trasmissione interspecie.
- Necessità di strategie di sorveglianza integrate:I risultati supportano la necessità di dare priorità ai roditori nei programmi di sorveglianza attiva e di implementare approcci integrati che combinino metagenomica, sierologia e monitoraggio ecologico nelle interfacce uomo-fauna selvatica.
Nel complesso, questo studio fornisce prove fondamentali a supporto dei sistemi di allerta precoce e dei quadri di valutazione del rischio per le malattie zoonotiche emergenti, rafforzando l'importanza della sorveglianza proattiva nelle regioni ad alto rischio.
Informazioni sul prodotto
Data di pubblicazione: 23 marzo 2026