Il 24 marzo 2026 si celebra la 31ª Giornata mondiale della tubercolosi. L'Organizzazione mondiale della sanità (OMS) ha annunciato il tema globale di quest'anno come“Sì! Possiamo sconfiggere la tubercolosi!”, sottolineando che una forte leadership governativa, un impegno politico costante e un'azione multisettoriale coordinata sono essenziali per porre fine all'epidemia di tubercolosi (TB).

Progressi globali e sfide rimanenti
Secondo il Rapporto globale sulla tubercolosi 2025, il controllo globale della tubercolosi ha raggiunto un traguardo significativo nel 2024, con entrambi iIncidenza e mortalità in caloper la prima volta dall'inizio della pandemia di COVID-19.
Un stimato10,7 milioni di personeNel 2024 si sono sviluppati casi di tubercolosi, di cui il 54% maschi, il 35% femmine e l'11% bambini e adolescenti. Tra questi casi, circa619.000 (5,8%)erano co-infettati da HIV e390.000 (3,6%)erano tubercolosi multiresistente o resistente alla rifampicina (MDR/RR-TB).
La tubercolosi ha causato circa1,23 milioni di mortinel 2024, rimanendo la principale causa infettiva di morte a livello globale, superando il COVID-19. Dopo tre anni di aumenti tra il 2021 e il 2023, l'incidenza globale della tubercolosi è diminuita di quasi il 2% nel 2024, riflettendo una graduale ripresa dei servizi per la tubercolosi.[1]
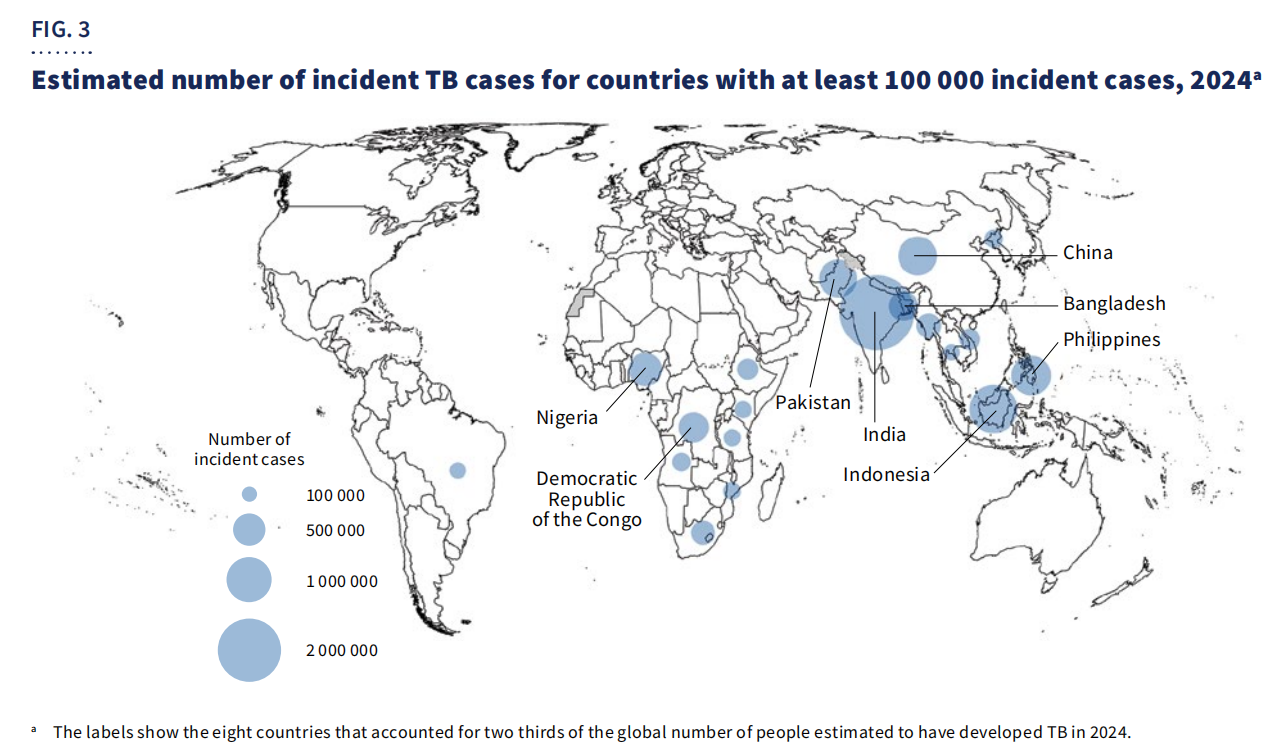
Dal punto di vista geografico,67% dei casierano concentrati in otto paesi: India, Indonesia, Filippine, Cina, Pakistan, Nigeria, Repubblica Democratica del Congo e Bangladesh.
Nonostante i progressi, la tubercolosi rimane una delle principali cause di morte tra le persone che vivono con l'HIV e un importante fattore che contribuisce alla mortalità associata alla resistenza antimicrobica. I finanziamenti globali continuano a essere insufficienti, con solo5,9 miliardi di dollaridisponibile nel 2024—ben al di sotto delobiettivo annuale di 22 miliardi di dollariprevisto per il 2027.
Questi dati evidenziano l'urgente necessità di rafforzare i programmi di controllo della tubercolosi a livello globale, concentrandosi sull'ampliamento dell'accesso alla diagnostica, sul miglioramento degli esiti del trattamento e sull'affrontare i determinanti sociali che favoriscono la trasmissione della tubercolosi. La lotta alla tubercolosi continua a richiedere una solida cooperazione internazionale e un impegno politico per raggiungere gli obiettivi della Strategia per porre fine alla tubercolosi.
Micobatterio tubercolare: patogenesi e classificazione
Il Mycobacterium tuberculosis (MTB/M. tuberculosis) è il principale e più comune agente patogeno responsabile della tubercolosi (TB). Può entrare nel corpo umano attraverso le vie respiratorie, il tratto digerente o la pelle e le mucose danneggiate, infettando più organi e causando diverse forme di TB. La TB polmonare, trasmessa principalmente tramite goccioline respiratorie, rappresenta oltre l'80% dei casi di TB. I sintomi comuni includono tosse, produzione di espettorato ed emottisi. Dopo l'infezione nei polmoni, i batteri possono diffondersi attraverso il flusso sanguigno a più sistemi, portando potenzialmente alla TB scheletrica, urinaria o gastrointestinale.[2]
Il MTB appartiene al genere Mycobacterium, che comprende:
- Complesso di Mycobacterium tuberculosis (MTBC): comprende, tra gli altri, M. tuberculosis, M. bovis, M. africanum, M. canettii e M. microti. Sebbene M. tuberculosis sia la causa principale della tubercolosi, anche M. bovis e M. africanum possono indurre la malattia.
- Micobatteri non tubercolari (NTM).
- Il Mycobacterium leprae è l'agente eziologico della lebbra.
Approcci diagnostici di laboratorio
Una diagnosi accurata e tempestiva è essenziale per un efficace controllo della tubercolosi. L'Organizzazione Mondiale della Sanità sottolinea cheLe tecnologie di diagnostica molecolare rapida hanno trasformato radicalmente la diagnosi della tubercolosi, consentendo l'identificazione altamente sensibile e specifica degli agenti patogeni e, al contempo, il rilevamento della resistenza ai farmaci.[1].
- Microscopia e colturae: La coltura batterica rimane il metodo di riferimento per la diagnosi di tubercolosi, in quanto consente l'identificazione definitiva di microrganismi vitali e supporta i test di sensibilità ai farmaci e l'analisi genomica. Tuttavia, a causa della lenta crescita del Mycobacterium tuberculosis, i risultati richiedono in genere dalle 2 alle 8 settimane, limitandone l'utilità clinica nelle decisioni urgenti.
-Test immunologici: I metodi immunologici, tra cui il test cutaneo alla tubercolina (TST) e i test di rilascio dell'interferone-gamma (IGRA), rilevano le risposte immunitarie dell'ospite all'infezione tubercolare. Sebbene utili per identificare l'infezione latente, questi test non sono in grado di distinguere in modo affidabile tra infezione attiva e pregressa e pertanto presentano una specificità diagnostica limitata in contesti ad alta prevalenza.
-Diagnostica molecolare (NAAT): I test basati sul DNA, come l'amplificazione degli acidi nucleici (NAAT), sono raccomandati per la loro elevata sensibilità e specificità.
-Sequenziamento mirato di nuova generazione (tNGS): Le tecnologie di sequenziamento mirato forniscono un'identificazione ad alta risoluzione delle mutazioni associate alla resistenza. Le linee guida dell'OMS raccomandano il tNGS come strumento avanzato per il rilevamento della resistenza ai farmaci dopo la diagnosi, a supporto delle strategie di trattamento di precisione [3].
-Sequenziamento metagenomico di nuova generazione (mNGS): Il sequenziamento metagenomico consente l'individuazione imparziale di un'ampia gamma di agenti patogeni senza necessità di previa selezione del bersaglio. Questo approccio è particolarmente prezioso in scenari clinici complessi o non chiari, come infezioni miste e pazienti immunocompromessi, dove le metodiche diagnostiche convenzionali possono risultare insufficienti.
L'OMS sottolinea inoltre che la conferma microbiologica è essenziale per avviare una terapia appropriata e migliorare gli esiti per i pazienti, rafforzando l'importanza di integrare la diagnostica molecolare avanzata nei programmi di controllo della tubercolosi [1].
Soluzioni complete di diagnostica molecolare da Macro & Micro-Test
1.Rilevamento della tubercolosi e della resistenza ai farmaci tramite PCR multiplexTubercolosi
| Codice prodotto | Nome del prodotto | Certificazione |
| HWTS-RT001 | Kit per la rilevazione del DNA del Mycobacterium Tuberculosis (PCR a fluorescenza) | CE |
| HWTS-RT137 | Kit per la rilevazione di mutazioni di resistenza all'isoniazide del Mycobacterium Tuberculosis (curva di fusione) | CE |
| HWTS-RT074 | Kit per la rilevazione della resistenza agli acidi nucleici e alla rifampicina del Mycobacterium Tuberculosis (curva di fusione) | CE |
| HWTS-RT102 | Kit per la rilevazione degli acidi nucleici basato sull'amplificazione isotermica della sonda enzimatica (EPIA) per il Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Kit per la rilevazione degli acidi nucleici del complesso Mycobacterium Tuberculosis liofilizzato (amplificazione isotermica con sonda enzimatica) | CE |
| HWTS-RT105 | Kit per la rilevazione del DNA di Mycobacterium Tuberculosis liofilizzato (PCR a fluorescenza) | CE |
| HWTS-RT147 | Kit per la rilevazione della resistenza agli acidi nucleici, alla rifampicina e all'isoniazide del Mycobacterium Tuberculosis (curva di fusione) | CE |
Quando sussiste un forte sospetto clinico di tubercolosi (TB), ilHWTS-RT147Il test è raccomandato per la rilevazione qualitativa dell'infezione da MTB e della tubercolosi multiresistente (MDR-TB). Questo test identifica le mutazioni nelgene rpoB, che portano alla resistenza alla rifampicina (RIF) e mutazioni nelgeni katG e InhAche sono associate alla resistenza all'isoniazide (INH). Fornisce un test efficiente e unico sia per MTB che per MDR-TB, incorporando un controllo di qualità interno per ridurre al minimo i risultati falsi negativi, garantendo risultati rapidi e accurati.
2.Sequenziamento mirato PTNseq per l'identificazione di patogeni respiratori e la profilazione della resistenza.
| Codice prodotto | Nome del prodotto | Specifiche |
| HWKF-TS0001 | Kit di arricchimento genico PTNseq per agenti patogeni responsabili di infezioni del flusso sanguigno | 24 test/kit |
| HWKF-TS0002 | Kit di arricchimento genico PTNseq per microrganismi patogeni responsabili di infezioni del sistema nervoso centrale. | 24 test/kit |
| HWKF-TS0003 | Kit di arricchimento genico PTNseq per agenti patogeni responsabili di infezioni respiratorie. | 24 test/kit |
| HWKF-AT0003 | Kit di costruzione automatizzata della libreria di arricchimento per microrganismi patogeni responsabili di infezioni respiratorie PTNseq (ONT) | 24 test/kit |
| HWKF-TS0004 | Kit di arricchimento genico PTNseq per patogeni infettivi ad ampio spettro | 24 test/kit |
| HWKF-TS0005 | Kit PTNseq per l'arricchimento genico di microrganismi patogeni infettivi ad ampio spettro | 24 test/kit |
| HWKF-TS0151 | Kit per la tipizzazione dei micobatteri e l'arricchimento dei geni di resistenza ai farmaci (metodo di amplificazione multipla) | 24 test/kit |
Nei casi di infezioni respiratorie miste (incluse infezioni delle vie respiratorie superiori e inferiori, tubercolosi e malattie respiratorie croniche), o quando è richiesta l'analisi del gene di resistenza ai farmaci (ad esempio, sospetta tubercolosi farmaco-resistente),Serie PTNseq di rilevamento genico mirato ad alta produttivitàpuò essere applicato. Basato su una tecnologia di sequenziamento mirato avanzata, PTNseq utilizza la PCR ultra-multiplex per arricchire sequenze target specifiche, combinata con il sequenziamento ad alto rendimento e la tecnologia nanopore di terza generazione per un'identificazione completa dei patogeni e la profilazione della resistenza ai farmaci.
Il sistema utilizza primer brevettati ad alta specificità per l'amplificazione ultra-multiplex dei geni target. Supportato da un database proprietario e da algoritmi bioinformatici intelligenti, fornisce un'accurata identificazione dei patogeni insieme all'analisi della resistenza ai farmaci e dei geni di virulenza. L'arricchimento mirato riduce l'interferenza del DNA dell'ospite, migliorando la sensibilità nei campioni con un elevato background umano e consentendo un rilevamento efficace di target difficili comeMicobatterio della tubercolosifunghi, batteri intracellulari, virus a RNA e geni di resistenza o virulenza.
PTNseq raggiunge un limite di rilevamentofino a 100 copie/mLe copre175 patogeni respiratori comuni, tra cui 76 batteri, 73 virus, 19 funghi, 7 micoplasmi, nonchéClamidia, Rickettsiae 54 geni di resistenza ai farmaci. Il pannello comprende ilMicobatterio della tubercolosiMicobatteri non tubercolari complessi e di maggiore importanza.
La serie PTNseq combina elevata sensibilità ed economicità, migliorando i tassi di rilevamento dei patogeni e supportando la terapia antimicrobica personalizzata, contribuendo al contempo a contrastare la resistenza antimicrobica. Integrata con il sistema completamente automatizzato di preparazione delle librerie per il sequenziamento genico (AIOS), offre una soluzione semplificata da utilizzare in ambito ospedaliero, con tempi di risposta rapidissimi, dal campione al risultato, a partire da sole 6,5 ore.

3. Sequenziamento metagenomico per l'individuazione di patogeni ad ampio spettro
| Codice prodotto | Nome del prodotto | Specifiche |
| HWKF-MN0011 | Kit per la rilevazione di agenti patogeni tramite metagenomica (DNA-Illumina) | 24 test/kit |
| HWKF-MN0018 | Kit per l'individuazione di agenti patogeni tramite metagenomica (DNA-MGI) | 24 test/kit |
| HWKF-MN0021 | Kit per la rilevazione di agenti patogeni tramite metagenomica (DNA-ONT) | 24 test/kit |
| HWKF-MN0012 | Kit per la rilevazione di agenti patogeni tramite metagenomica (RNA-Illumina) | 24 test/kit |
| HWKF-MN0019 | Kit per la rilevazione di agenti patogeni mediante metagenomica (RNA-MGI) | 24 test/kit |
| HWKF-MN0022 | Kit per la rilevazione di agenti patogeni tramite metagenomica (RNA-ONT) | 24 test/kit |
| HWKF-MN0013 | Kit per la rilevazione di agenti patogeni tramite metagenomica (DNA+RNA-Illumina) | 24 test/kit |
| HWKF-AYM0013 | Kit per la costruzione automatizzata di librerie per il rilevamento metagenomico di agenti patogeni (DNA+RNA-Illumina) | 24 test/kit |
| HWKF-MN0020 | Kit per la rilevazione di agenti patogeni mediante metagenomica (DNA+RNA-MGI) | 24 test/kit |
| HWKF-MN0023 | Kit per la rilevazione di agenti patogeni tramite metagenomica (DNA+RNA-ONT) | 24 test/kit |
Quando la diagnosi clinica non è chiara,Rilevamento genico ad alta produttività di agenti patogeni mNGSpuò essere eseguito su vari campioni del paziente, tra cui liquido di lavaggio broncoalveolare, espettorato, tamponi faringei, sangue, versamento pleurico, pus e campioni di tessuto. Questo approccio utilizza la tecnologia di sequenziamento metagenomico, in cui diversi campioni vengono sottoposti a un pretrattamento mirato seguito dall'estrazione di acidi nucleici utilizzando microsfere di vetro ed enzimi digestivi della parete, migliorando l'efficienza di estrazione. Il sequenziamento è adattato a più piattaforme, garantendo un elevato volume di dati per una migliore sensibilità mNGS e integrità dell'assemblaggio. I dati vengono analizzati utilizzando un database autocostruito e algoritmi intelligenti per rilevareoltre 20.000 agenti patogeni, inclusi batteri, funghi, virus e parassiti, fornendo informazioni su microrganismi patogeni sospetti. Questo metodo è adatto per pazienti difficili da diagnosticare, in condizioni critiche o immunocompromessi, compresa l'identificazione diMTBcomplessoENTM, nonché infezioni miste. Migliora significativamente i tassi di rilevamento dei patogeni e contribuisce a guidare l'uso mirato degli antibiotici in ambito clinico, consentendo una diagnosi precisa dell'infezione.
Conclusione
Nonostante i notevoli progressi compiuti, la tubercolosi rimane una delle principali sfide per la salute globale, soprattutto nel contesto della resistenza ai farmaci, delle carenze di finanziamento e dell'accesso ineguale alla diagnostica.
L'OMS sottolinea che ampliare l'accesso alla diagnostica molecolare rapida e alle tecnologie di sequenziamento avanzate è essenziale per raggiungere gli obiettivi della Strategia per porre fine alla tubercolosi. Grazie alla continua innovazione, agli investimenti e alla collaborazione globale, porre fine alla tubercolosi non è più un'aspirazione, ma un obiettivo raggiungibile.
Riferimenti:
- Organizzazione Mondiale della Sanità. Rapporto globale sulla tubercolosi 2024/2025: Diagnosi, test e trattamento.
- Organizzazione Mondiale della Sanità. Manuale dell'OMS per la selezione dei test diagnostici rapidi molecolari raccomandati dall'OMS per l'individuazione della tubercolosi e della tubercolosi farmaco-resistente.
- Organizzazione Mondiale della Sanità. Linee guida consolidate dell'OMS sulla tubercolosi: Modulo 3 – Diagnosi (aggiornamento 2024).
Data di pubblicazione: 24 marzo 2026
