I. Panoramica delESMOLinee guida 2025
Nell'agosto 2025, l'ESMO ha pubblicato ufficialmente le Linee guida di pratica clinica ESMO per la diagnosi, il trattamento e il follow-up del carcinoma polmonare non a piccole cellule in fase iniziale e localmente avanzato, sulla prestigiosa rivista oncologica Annals of Oncology. Si tratta del primo aggiornamento completo dalla versione del 2017 e rappresenta un riferimento estremamente autorevole per gli oncologi di tutto il mondo.

Il tumore al polmone è la neoplasia con la più alta incidenza e mortalità a livello globale. Ogni anno si registrano oltre 2,2 milioni di nuovi casi e più di 1,8 milioni di decessi, il che rende il tumore al polmone la principale causa di morte per cancro sia negli uomini che nelle donne. Il carcinoma polmonare non a piccole cellule (NSCLC) rappresenta circa l'80-85% di tutti i casi di tumore al polmone. In questo contesto critico, la pubblicazione delle linee guida del 2025 apporta un nuovo impulso scientifico alla pratica clinica, con un aggiornamento particolarmente importante sulle strategie di test dei biomarcatori.
II. Interpretazione dei principali aggiornamenti delle linee guida
2.1 Test dei biomarcatori: da “opzionale” a “essenziale”
Le linee guida del 2025 rappresentano un importante passo avanti strategico per quanto riguarda i test sui biomarcatori. Le linee guida affermano esplicitamente che i test sui biomarcatori sono essenziali per le decisioni terapeutiche nei pazienti con NSCLC in stadio IB-III.
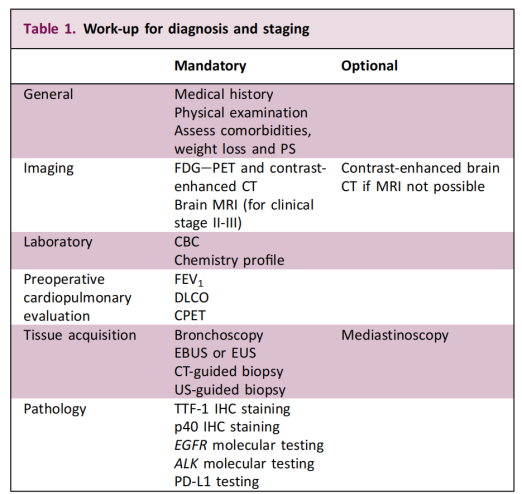
Questa raccomandazione estende l'ambito dei test molecolari, precedentemente focalizzati sui pazienti con malattia in stadio avanzato, anche ai casi in fase iniziale e resecabili. L'obiettivo principale è identificare le mutazioni genetiche responsabili della progressione della malattia e fornire una base scientifica per un trattamento di precisione personalizzato. La linea guida sottolinea inoltre che la fattibilità della biopsia e l'approccio diagnostico devono essere determinati da un team multidisciplinare sulla base delle caratteristiche del paziente e del tumore.
Per quanto riguarda la specifica strategia di test, la linea guida raccomanda chiaramente di eseguire i test genetici prima di prendere decisioni chirurgiche e che questi includano almeno EGFR e ALK. Questo concetto di "test preventivo" ha una profonda rilevanza clinica per la stratificazione precisa e il trattamento personalizzato del NSCLC in stadio iniziale: la tempestività e l'accuratezza dei risultati dei test determinano direttamente la scelta della successiva terapia adiuvante.
2.2 Progressi terapeutici nel carcinoma polmonare non a piccole cellule in stadio iniziale positivo per oncogeni driver
Le linee guida del 2025 integrano i dati provenienti da numerosi studi clinici di rilievo per definire un percorso di trattamento di precisione chiaro per i pazienti affetti da NSCLC in stadio iniziale positivo agli oncogeni driver.
Pazienti positivi alla mutazione EGFR:Sulla base dello studio ADAURA, un punto di riferimento fondamentale, la terapia adiuvante postoperatoria con osimertinib per tre anni è diventata lo standard di cura globale per i pazienti con delezione dell'esone 19 o mutazione L858R dell'esone 21 del gene EGFR. Lo studio ADAURA è uno studio internazionale, multicentrico, randomizzato e controllato di fase III che ha valutato l'efficacia e la sicurezza dell'osimertinib adiuvante in pazienti con NSCLC in stadio IB-IIIA con mutazione del gene EGFR, sottoposti a resezione completa. Lo studio ha dimostrato che l'osimertinib ha migliorato significativamente sia la sopravvivenza libera da malattia che la sopravvivenza globale rispetto al placebo, stabilendo l'osimertinib come nuovo standard di cura per questa popolazione. Tuttavia, analisi esplorative dello studio ADAURA hanno indicato che circa il 36% delle interruzioni precoci del trattamento è stato causato da eventi avversi e un altro 31% da decisioni del paziente. Questo dato sottolinea la necessità di test basali accurati prima del trattamento per garantire che la terapia mirata venga somministrata ai pazienti che possono trarne un beneficio duraturo.
Pazienti ALK-positivi:Sulla base dello studio ALINA, l'alectinib adiuvante postoperatorio per due anni è ora lo standard di cura. Nell'analisi primaria dello studio ALINA, uno studio randomizzato in aperto di fase III, l'alectinib ha mostrato un marcato beneficio in termini di sopravvivenza libera da malattia nella popolazione in stadio II-IIIA, con un hazard ratio di 0,24. Dati aggiornati dello studio ALINA, presentati al congresso ESMO 2025, hanno mostrato che dopo ≥3 anni di follow-up, il beneficio in termini di sopravvivenza libera da malattia dell'alectinib è rimasto "sostenuto e clinicamente significativo", con un hazard ratio di 0,36 nella popolazione in stadio II-IIIA. L'ultimo tasso di sopravvivenza globale a 4 anni riportato ha raggiunto il 98,4%, il tasso di sopravvivenza libera da malattia a 4 anni è stato del 75,5% e anche la sopravvivenza libera da malattia a carico del sistema nervoso centrale è risultata migliorata, senza nuovi segnali di sicurezza. Questi dati solidi consolidano ulteriormente l'alectinib adiuvante come standard di cura dopo la resezione del NSCLC ALK-positivo e sottolineano l'importanza di test accurati per identificare tali pazienti.
Scelta del metodo di prova:La linea guida ESMO del 2025 elenca esplicitamenteTest di pannello RT-PCR multiplexInsieme a NGS basato su RNA, IHC e FISH, questo approccio tecnico è raccomandato per la rilevazione della fusione ALK. Ciò indica che il requisito fondamentale della linea guida è quello di eseguire test per orientare le decisioni cliniche, piuttosto che imporre una piattaforma di test specifica. Per i prodotti RT-PCR focalizzati sulla rilevazione di EGFR e ALK, questa strategia di test flessibile fornisce una solida giustificazione, basata sulle linee guida, per il loro utilizzo nella pratica clinica.
III. Soluzioni tecniche per test di precisione
Le linee guida del 2025 anticipano l'esecuzione dei test alla fase decisionale pre-operatoria, innalzando gli standard di accuratezza, sensibilità e accessibilità delle analisi. I due prodotti di rilevamento basati sulla RT-PCR descritti di seguito sono perfettamente conformi ai requisiti delle linee guida dal punto di vista tecnico.
3.1 Kit per la rilevazione delle mutazioni EGFR – Piattaforma tecnologica ARMS avanzata
Tecnologia di baseLa tecnologia ARMS avanzata consente l'amplificazione specifica di sequenze mutanti a bassa abbondanza in presenza di un elevato background di tipo selvatico.
Tre misure di sicurezza tecniche:
-ARMS migliorato → migliora il riconoscimento delle mutazioni
- Arricchimento enzimatico → digerisce il background di tipo selvatico e arricchisce le sequenze mutanti
-Blocco termico → sopprime l'amplificazione non specifica
Prestazione: Sensibilità diFrequenza dell'allele mutante dell'1%
Controllo della contaminazioneControllo interno integrato + enzimi UNG per prevenire la contaminazione
Tempi di consegna: Funzionamento a tubo chiuso, circa120 minuti
Compatibilità del campione:Tessuto/biopsia liquidacampioni → affronta il requisito di “testare in anticipo”
Copertura:45 mutazioninegli esoni 18-21 dell'EGFR, corrispondenti precisamente alle regioni evidenziate dalle linee guida (delezioni dell'esone 19 e L858R dell'esone 21)
Uso clinicoGuida direttamente la terapia con EGFR-TKI
3.2 MMT Kit per la rilevazione della fusione EML4-ALK – Soluzione per la rilevazione della fusione basata sull'RNA

-Piattaforma tecnologica: La RT-PCR basata sull'RNA offre vantaggi intrinseci rispetto ai metodi basati sul DNA per il rilevamento delle fusioni
-Vantaggio basato sull'RNA: Rileva direttamente le trascrizioni di fusione espresse, evitando efficacemente i falsi negativi
-Prove dello studioNelle fusioni ALK a bassa frequenza, la RT-PCR è significativamente più affidabile dei test basati sul DNA.
-Sensibilità: Rileva fusioni fino a20 copie per reazione
-Copertura delle varianti: Copertine12 varianti comuni della fusione EML4-ALK(inclusa la variante 1 ~33%; le varianti 3a/3b insieme ~29%)
-Controllo operativo e della contaminazione: Tubo chiuso, ~120 minuti; controlli di processo integrati + enzima UNG prevengono risultati falsi
-Compatibilità degli strumentiCompatibile con diversi strumenti PCR in tempo reale di uso comune.
-Allineamento delle linee guidaAltamente conforme alle linee guida ESMO
IV. Coerenza tra i test e le raccomandazioni delle linee guida
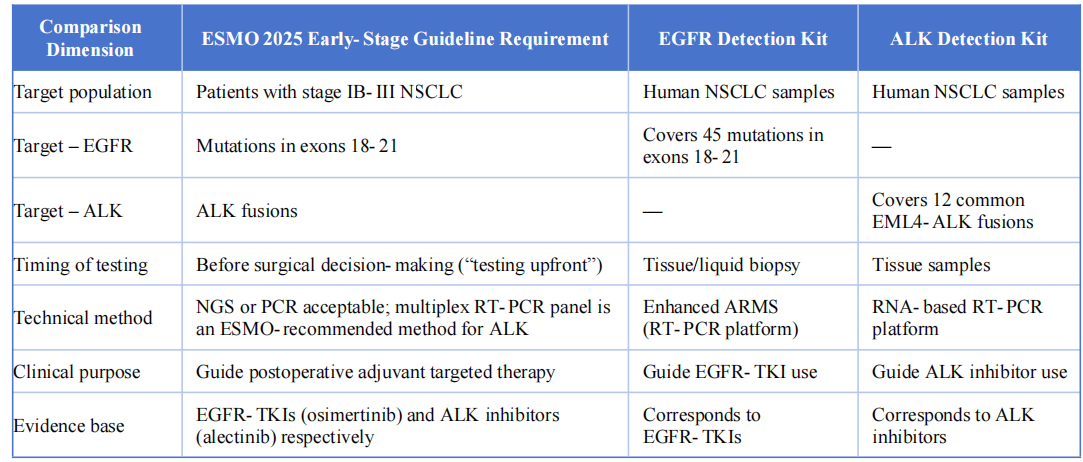
I due prodotti di rilevamento sono altamente conformi alle linee guida ESMO 2025 per il carcinoma polmonare non a piccole cellule in fase iniziale e localmente avanzato, per quanto riguarda le seguenti dimensioni chiave:
V. Conclusion
Le linee guida ESMO 2025 per il NSCLC in fase iniziale inaugurano una nuova era di diagnosi e trattamento di precisione, incentrata su “Test preliminari, individuazione precisa del bersaglio e ottimizzazione del trattamento."Il kit per il rilevamento delle mutazioni EGFR e il kit per il rilevamento della fusione MMT EML4-ALK soddisfano i requisiti delle linee guida in termini di target, tempistica e accuratezza, attraverso percorsi tecnici distinti."
Il kit EGFR utilizza una tecnologia ARMS avanzata per il rilevamento ad alta sensibilità di mutazioni mirate in campioni limitati, supportando sia la biopsia tissutale che quella liquida per consentire "test preliminari".
Il kit ALK si basa sulla RT-PCR a base di RNA, offrendo vantaggi rispetto ai metodi basati sul DNA per il rilevamento delle fusioni, in linea con la raccomandazione dell'ESMO di utilizzare pannelli RT-PCR multiplex per il test ALK.
Insieme, questi due prodotti costituiscono una soluzione di test di precisione conforme alle linee guida ESMO 2025, a supporto della terapia adiuvante personalizzata per il carcinoma polmonare non a piccole cellule in fase iniziale.
Riferimenti:
- Zer A, Ahn MJ, Barlesi F, et al. Carcinoma polmonare non a piccole cellule in fase iniziale e localmente avanzato: Linee guida di pratica clinica ESMO per la diagnosi, il trattamento e il follow-up. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Data di pubblicazione: 6 maggio 2026

