Resistenza agli acidi nucleici e alla rifampicina del Mycobacterium Tuberculosis
Nome del prodotto
Kit HWTS-RT074B per la rilevazione della resistenza agli acidi nucleici e alla rifampicina del Mycobacterium Tuberculosis (curva di fusione)
Certificato
CE
Epidemiologia
Il Mycobacterium tuberculosis, noto anche come bacillo della tubercolosi (TB), è il batterio patogeno che causa la tubercolosi. Attualmente, i farmaci antitubercolari di prima linea comunemente utilizzati includono isoniazide, rifampicina ed esametolo. I farmaci antitubercolari di seconda linea includono fluorochinoloni, amikacina e kanamicina. Tra i farmaci di recente sviluppo si annoverano linezolid, bedaquilina e delamani. Tuttavia, a causa dell'uso scorretto dei farmaci antitubercolari e delle caratteristiche della struttura della parete cellulare del Mycobacterium tuberculosis, quest'ultimo sviluppa resistenza ai farmaci antitubercolari, il che rappresenta una seria sfida per la prevenzione e il trattamento della tubercolosi.
La rifampicina è ampiamente utilizzata nel trattamento dei pazienti affetti da tubercolosi polmonare dalla fine degli anni '70, con risultati significativi. È stata la prima scelta per abbreviare la durata della chemioterapia in questi pazienti. La resistenza alla rifampicina è principalmente causata dalla mutazione del gene rpoB. Nonostante la continua introduzione di nuovi farmaci antitubercolari e il miglioramento clinico nel trattamento della tubercolosi polmonare, la carenza di farmaci antitubercolari rappresenta ancora un problema, e il fenomeno dell'uso irrazionale dei farmaci in ambito clinico è piuttosto diffuso. È evidente che l'eliminazione completa del Mycobacterium tuberculosis nei pazienti affetti da tubercolosi polmonare non è sempre efficace, il che porta allo sviluppo di diversi gradi di resistenza ai farmaci, prolungando il decorso della malattia e aumentando il rischio di mortalità.
Canale
| Canale | Canali e fluorofori | Tampone di reazione A | Tampone di reazione B | Tampone di reazione C |
| Canale FAM | Reporter: FAM, Quencher: Nessuno | rpoB 507-514 | rpoB 513-520 | 38KD e IS6110 |
| Canale CY5 | Reporter: CY5, Estintore: Nessuno | rpoB 520-527 | rpoB 527-533 | / |
| Canale HEX (VIC) | Reporter: HEX (VIC), Quencher: Nessuno | controllo interno | controllo interno | controllo interno |
Parametri tecnici
| Magazzinaggio | ≤-18℃ Al buio |
| durata di conservazione | 12 mesi |
| Tipo di campione | Espettorato |
| CV | ≤5,0% |
| LoD | micobatterio tubercolare 50 batteri/mL tipo selvatico resistente alla rifampicina: 2x103batteri/mL mutante omozigote: 2x103batteri/mL |
| Specificità | Rileva il Mycobacterium tuberculosis di tipo selvatico e i siti di mutazione di altri geni di resistenza ai farmaci come katG 315G>C\A, InhA-15C> T; i risultati del test non mostrano resistenza alla rifampicina, il che significa che non vi è reattività crociata. |
| Strumenti applicabili: | Sistemi PCR in tempo reale SLAN-96P Sistema PCR in tempo reale BioRad CFX96 Sistema PCR in tempo reale LightCycler480® |
Flusso di lavoro
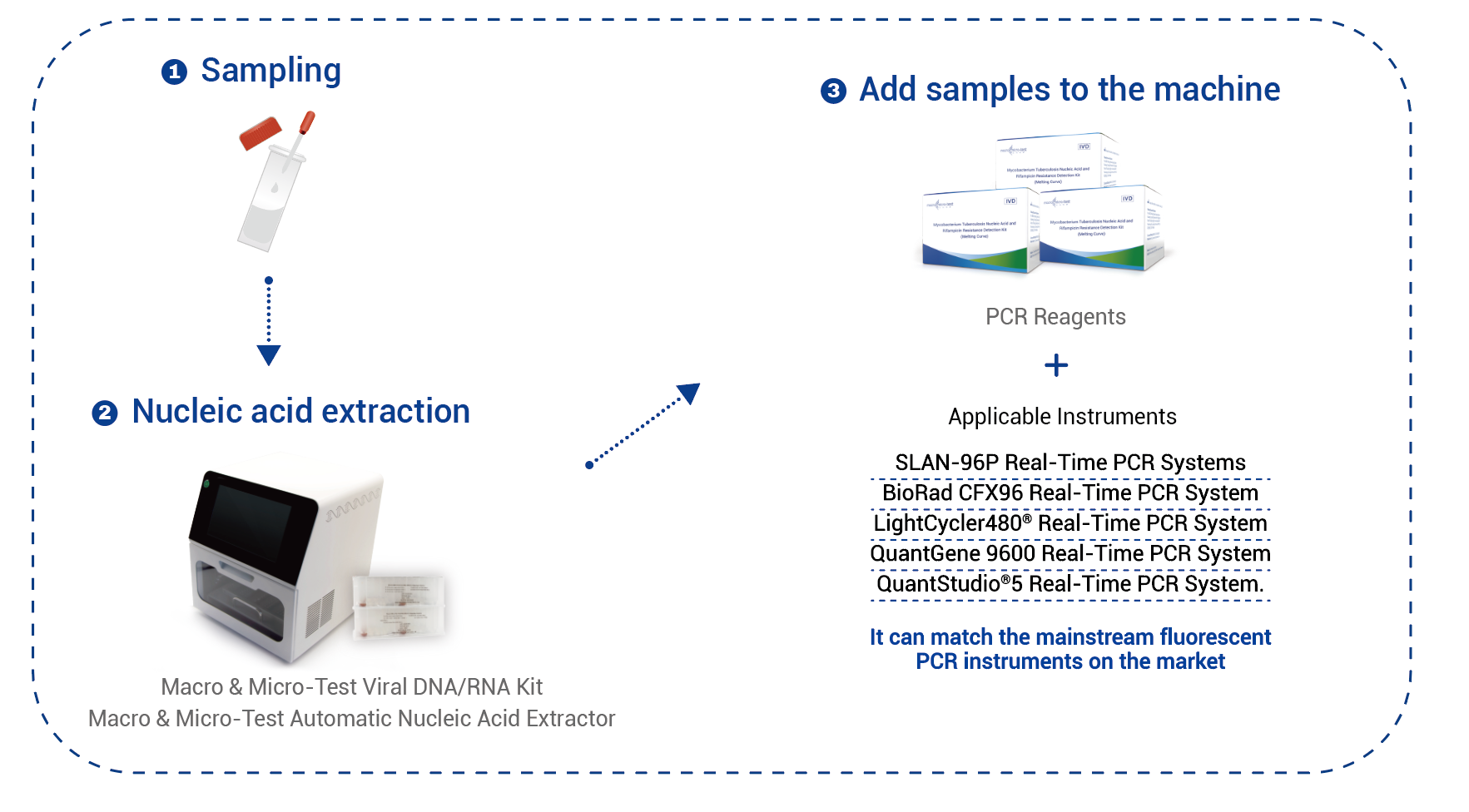
Se si utilizza il kit Macro & Micro-Test General DNA/RNA (HWTS-3019-50, HWTS-3019-32, HWTS-3019-48, HWTS-3019-96) (utilizzabile con l'estrattore automatico di acidi nucleici Macro & Micro-Test (HWTS-3006C, HWTS-3006B)) o la colonna Macro & Micro-Test Viral DNA/RNA (HWTS-3022-50) di Jiangsu Macro & Micro-Test Med-Tech Co., Ltd. per l'estrazione, aggiungere in sequenza 200 μL di controllo positivo, controllo negativo e campione di espettorato trattato da analizzare, e aggiungere separatamente 10 μL di controllo interno al controllo positivo, al controllo negativo e al campione di espettorato trattato da analizzare. I passaggi successivi devono essere eseguiti rigorosamente secondo le istruzioni di estrazione. Il volume del campione estratto è di 200 μL e il volume di eluizione raccomandato è di 100 μL.